作者:安法醫新抗老科學研究中心 研發長 吳杰浩
(歡迎分享與引用,請註明出處:安法醫新抗老科學研究中心,謝謝)
從MSC作用機制到研究發展,重新理解現代再生醫學的核心邏輯
近年來,隨著再生醫學與細胞科學持續進步,幹細胞相關研究已逐步從基礎實驗延伸至更多轉譯醫學與健康科學領域,並成為當代生命科學與精準醫學中備受關注的重要方向之一。從組織修復機制、免疫調節研究、慢性發炎調控,到近年受到高度重視的老化科學與健康管理議題,幹細胞所代表的,已不僅是一項新興生物技術,更被視為未來精準醫療與再生科學的重要發展基礎。
然而,在大眾對幹細胞議題關注持續提升的同時,關於不同細胞來源的討論也日益增加。尤其在接觸相關資訊時,許多人最常提出的問題,往往集中於細胞來源本身。
例如,來自自身組織的自體細胞與來自健康供體的異體細胞究竟有何差異?年輕供體來源是否代表更佳細胞品質?異體細胞的免疫相容性又應如何理解?
事實上,若從現代再生醫學與細胞生物學角度來看,這些問題並無絕對單一的判斷標準。細胞技術的發展與應用評估,從來不僅取決於「來源」本身,而更涉及細胞品質、生物活性、製備條件、功能完整性及應用目的等多重因素的綜合考量。
幹細胞療效的核心,早已不只是「補充細胞」
目前再生醫療領域最常使用的細胞類型之一,是所謂的間充質幹細胞(Mesenchymal Stem/Stromal Cells, MSC)。MSC廣泛存在於人體多種組織中,包括骨髓、脂肪、臍帶與胎盤等,因其具備多向分化能力與良好培養特性,而成為現代細胞治療最重要的研究與應用對象。
早期醫學界曾普遍認為,幹細胞治療的原理是將細胞輸入人體後,使其直接分化為新的組織細胞,以取代受損或老化細胞。然而,近十餘年的研究逐漸發現,MSC真正發揮治療效果的關鍵,並非單純來自「分化替代」,而更主要是透過其強大的旁分泌(Paracrine)與微環境調節能力。
換句話說,MSC在人體內更像是一個高度活躍的「生物訊號調節者」。
其可分泌大量生長因子、細胞激素、趨化因子與細胞外囊泡(如外泌體),透過這些訊號分子與周圍細胞進行溝通,進一步達到刺激組織修復、調節免疫反應、抑制慢性發炎、促進血管新生與改善局部微環境等多重作用。正因如此,MSC領域的重要學者 Arnold Caplan 教授甚至提出,MSC更應被重新定義為 Medicinal Signaling Cells(醫療訊號細胞),而非僅僅是傳統認知中的「幹細胞」。這項觀念的改變,也重新定義了整個再生醫學產業對幹細胞的理解。
為何MSC被視為現代再生醫學的重要工具?
MSC之所以受到高度關注,除了其具備基本再生潛能外,更重要的是它同時具備多重生理調節功能。
首先,是其免疫調節能力。MSC可透過影響T細胞、B細胞、自然殺手細胞(NK cell)、巨噬細胞與樹突細胞等多種免疫細胞活性,幫助調節人體免疫反應平衡,因此在慢性發炎、自體免疫疾病及免疫失衡相關疾病中皆具有高度研究價值。
其次,是其抗發炎與微環境重建能力。MSC能透過調控多種促炎與抗炎因子,降低局部發炎反應與氧化壓力,並協助建立更適合組織修復的微環境。
此外,其分泌之 VEGF、FGF、HGF 等生長因子,亦可進一步促進血管新生與局部循環改善,提升組織供氧與營養供應,為整體修復創造更佳條件。
因此,從現代觀點來看,MSC的價值早已不只是「補細胞」,而更像是:
透過調節、活化與重建人體內在修復系統,來間接促進整體生理平衡與再生。
自體與異體幹細胞:差異究竟在哪?
所謂自體幹細胞,是指取自患者自身的細胞來源,例如自體脂肪或骨髓來源細胞。由於細胞與患者基因背景完全一致,因此理論上具有最佳免疫相容性,通常較不易產生明顯免疫辨識問題,亦符合高度個體化醫療的概念。
而異體幹細胞,則是來自其他健康供體,例如臍帶、胎盤或經篩選之健康成人捐贈者。其主要優勢在於可選擇年輕、健康且細胞品質穩定的供體來源,並可透過標準化製程進行大量培養與品質控制。
然而,這並不代表兩者存在絕對優劣之分。
年輕供體細胞是否一定更好?
這是臨床上最常見的迷思之一。
從細胞生物學角度來說,年輕供體來源細胞通常確實具備:
較佳增殖能力、更低衰老比例、更高代謝活性與較佳旁分泌能力,因此理論上具備一定生物學優勢。
但臨床效果從來不是只由「年齡」決定。
真正影響細胞治療效果的,往往還包括:
細胞活性是否足夠、純度是否穩定、製備過程是否標準化、培養代數是否適當、保存及復甦流程是否完善,以及整體治療設計與劑量規劃是否合理。
因此:
來源年輕僅代表潛在優勢之一,並不等於臨床效果必然更佳。
同樣地,自體細胞也不代表一定品質較差。即便年齡增加可能影響幹細胞活性,但細胞品質仍同時受到慢性疾病、代謝狀態、發炎程度、生活型態與整體健康管理等因素影響。許多健康管理良好的中壯年族群,其自體細胞品質仍可維持於相當良好水準。
異體幹細胞真的完全不排斥嗎?
另一個常見誤解,是認為MSC屬於「免疫特權細胞」,因此異體使用完全不會排斥。但實際上,近年學界已修正此觀念。更準確地說,MSC應被定義為:
低免疫原性(Low Immunogenicity)細胞,而非完全免疫豁免。
也就是說,相較一般異體移植細胞,MSC較不容易引發劇烈免疫排斥反應,但仍可能被宿主免疫系統辨識與逐步清除。因此異體細胞並非「絕對不排斥」,而是「整體耐受性較佳」。
真正決定療效的,從來不是來源,而是品質
當前再生醫學最核心的觀念之一,即是:
細胞治療的效果,真正取決於功能與品質,而非單純來源。
臨床上真正值得關注的問題,不是單純問「自體好還是異體好」,而應進一步評估:
- 細胞是否具備足夠活性?
- 是否保有完整旁分泌能力?
- 是否具備穩定免疫調節功能?
- 是否經過良好品質控制與標準化製備?
- 是否適合患者本身狀態與治療需求?
因為即使來源再好,若細胞本身品質不佳、活性不足或製備流程不完善,其最終效果亦將大打折扣。
結語
整體而言,自體與異體幹細胞各具優勢,並不存在絕對優劣之分。現代再生醫學真正關注的核心,早已不只是「細胞來自哪裡」,而是:
細胞品質是否足夠優良、功能是否完整、治療設計是否精準,以及是否真正符合個體需求。
未來幹細胞治療的發展方向,也將從單純比較來源,逐步走向:
高品質細胞製造 × 精準治療設計 × 個體化健康管理整合
唯有建立在完整科學基礎與嚴謹品質控管之上,才能真正發揮再生醫學的長期價值。
文獻參考
- Mesenchymal Stem Cells: Time to Change the Name! Stem Cells Transl Med.2017 Jun;6(6):1445-1451.
- Concise Review: Mesenchymal Stem Cells: From Roots to Boost. Stem Cells. 2019 Jul;37(7):855-864.
- Mesenchymal stem cells: immune evasive, not immune privileged. Nat Biotechnol. 2014 Mar;32(3):252-60.
- Mesenchymal Stem Cell Secretome: Toward Cell-Free Therapeutic Strategies in Regenerative Medicine. Int J Mol Sci. 2017 Aug 25;18(9):1852.
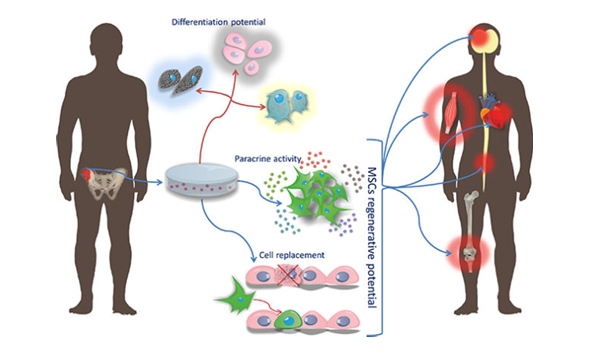
圖一: 間質幹細胞(MSC)可透過分化潛能、旁分泌訊號與免疫調節等多重機制,促進受損組織修復並支持全身多器官再生與功能改善。(圖片來源: Stem Cells. 2019 July ; 37(7): 855–864.)

