作者:安法醫新抗老科學研究中心 研發長 吳杰浩
(歡迎分享與引用,請註明出處:安法醫新抗老科學研究中心,謝謝)
衰老、心血管疾病、神經退行性疾病,甚至癌症化療後的器官損傷,背後其實常常指向同一個核心問題——線粒體功能衰退。
線粒體被稱為細胞的“發電廠”,一旦數量減少或功能下降,細胞就會陷入能量不足、氧化壓力升高、修復能力減弱的惡性循環。過去幾十年,醫學界嘗試用藥物刺激線粒體生成,但效果短暫、需要反復給藥,始終難以真正解決問題。
2025 年,美國德州農工大學團隊在《美國國家科學院院刊(PNAS)》發表的一項研究,提出了一條全新的思路:不是修復受損細胞,而是先訓練“健康細胞”成為線粒體工廠,再把新的線粒體“送”過去。
一、細胞其實會“互相支援”,只是效率太低
近年來,科學家發現細胞之間存在一種天然現象,稱為線粒體轉移(intercellular mitochondrial transfer)。
當某些細胞能量不足時,鄰近的健康細胞可以通過細胞間通道,將線粒體傳遞過去,幫助其恢復功能。
問題在於——
這種轉移效率非常低,遠不足以應對疾病或衰老造成的大規模損傷。
二、研究突破:把幹細胞變成“線粒體工廠”
這項研究的關鍵創新,在於引入了一種具有原子缺陷結構的二硫化鉬納米材料(MoS₂ nanoflowers)。
研究人員並沒有直接把納米材料用在受損細胞上,而是先將其用於間充質幹細胞(MSC):
- 納米花進入幹細胞後
- 清除過量活性氧(ROS)
- 啟動 SIRT1–PGC-1α–TFAM 這一經典的線粒體生合成通路
結果是:
➡ 幹細胞內線粒體數量顯著增加(mtDNA 約提升 2 倍)
➡ ATP 生成與線粒體呼吸能力明顯增強
這些幹細胞,被作者形象地稱為:
“線粒體生物工廠(Mitochondrial Biofactories)”
三、關鍵不是“製造”,而是“傳遞”
當這些“線粒體工廠型”幹細胞與受損細胞共培養時,研究人員觀察到:
- 線粒體通過隧道樣納米管(Tunneling Nanotubes, TNTs)直接轉移
- 轉移效率提升 2–4 倍
- 明確排除了“只是染料或納米材料轉移”的可能
更重要的是,這些被轉移的線粒體並不是“擺設”,而是真正整合進受體細胞的線粒體網路中,持續參與能量代謝。
四、在損傷模型中,幾乎實現“能量重啟”
研究進一步在多種損傷模型中驗證了效果,包括:
- 線粒體呼吸鏈抑制
- 化療藥物(如 Doxorubicin)誘導的心臟細胞損傷
結果顯示,接受線粒體轉移的細胞:
- ATP 水準顯著恢復
- 氧化壓力下降
- 凋亡與細胞死亡明顯減少
研究團隊形容這一過程就像:
“給細胞換一塊新電池,而不是修一塊舊電池。”
五、這項研究意味著什麼?
這項工作的重要性,不在於某一種材料本身,而在於它提出了一種全新的治療邏輯:
- 不依賴基因改造
- 不需要長期用藥
- 利用並放大身體本就存在的修復機制
未來潛在應用方向包括:
- 抗衰老醫學
- 心血管與神經退行性疾病
- 癌症治療相關的器官保護
- 線粒體疾病與代謝異常
當然,目前研究仍停留在實驗室階段,距離臨床應用仍需安全性與動物實驗驗證。但可以確定的是,“以線粒體為核心的細胞修復策略”,正在成為再生醫學與抗衰老領域的重要新方向。
参考文献
Soukar J. et al. Nanomaterial-induced mitochondrial biogenesis enhances intercellular mitochondrial transfer efficiency.
PNAS 2025 Vol. 122 No. 43 e2505237122
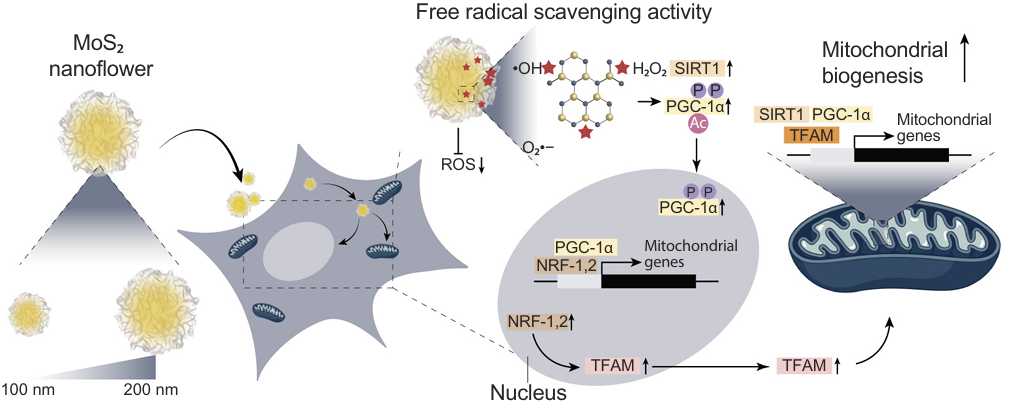
Vacancy-rich MoS₂ nanoflowers activate the SIRT1–PGC-1α pathway, promoting mitochondrial biogenesis and enhancing cellular bioenergetics, thereby converting MSCs into mitochondrial biofactories.
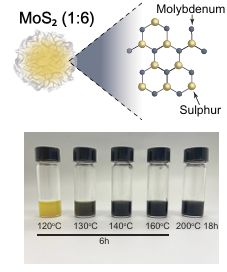

具有原子缺陷結構的二硫化鉬納米材料(MoS₂ nanoflowers)。
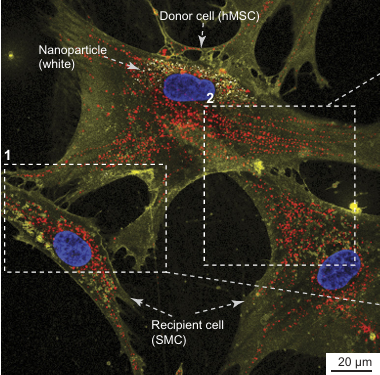
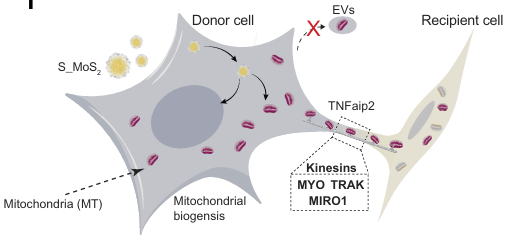
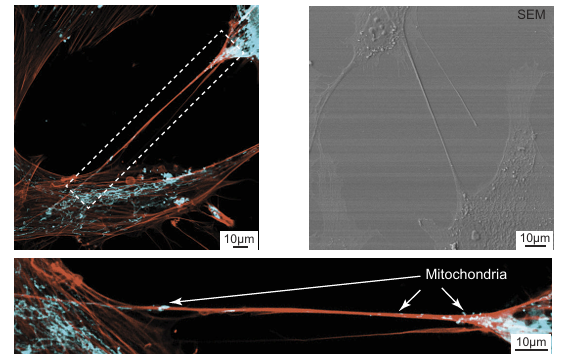
線粒體通過隧道樣納米管(Tunneling Nanotubes, TNTs)直接轉移

